一、同分异构体
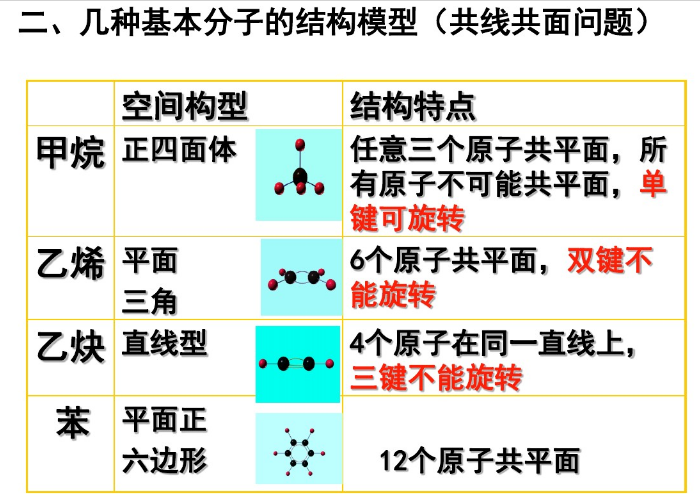
二、几种基本分子的结构模型(共线共面问题)
三、有机物重要物理性质
四、有机物的化学性质
(一)官能团的性质
(二)常见有机物之间的转化关系
(三)有机化学反应类型
(四)反应条件小结
五、常见的有机实验、有机物分离提纯
六、有机推断合成的一般思路
七、有机计算

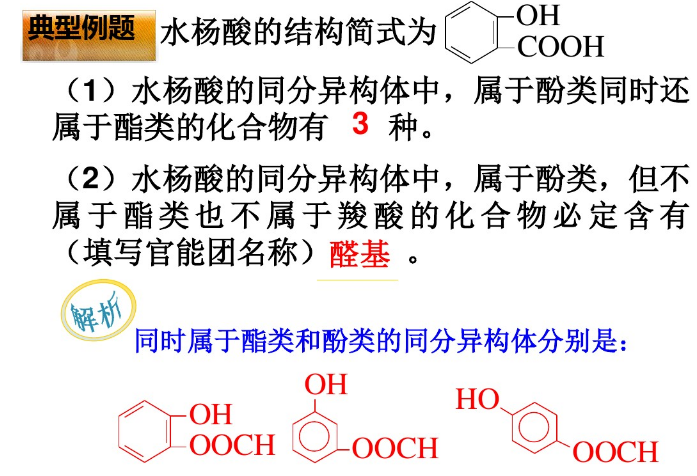
[小结]同分异构体的书写的基本方法1、判类别:根据分子式确定官能团异构(类别异构)
2、写碳链:主链由长到短,支链由简到繁,位置由心到边,排列邻、间、对。
3、移官位:变换官能团的位置(若是对称的,依次书写不可重复)
4、氢饱和:按“碳四键”原理,碳原子剩余的价键用氢原子去饱和。
三、有机物重要物理性质
状态
・n≤4的烃、新戊烷、甲醛、一氯甲烷、一氯乙烷、一溴甲烷常温呈气态,
・低级(+碳以下)的醇、醛、酸、酯常温呈液态
・苯酚,草酸,苯甲酸、硬脂酸,软脂酸常温呈固;密度
・比水轻:所有烃类(包括苯及其同系物)、酯(如乙酸乙酯)、油脂
・比水重:硝基苯、溴苯、CC14、溴乙烷及大多数卤代烃、液态苯酚
溶解性
・有机物均能溶于有机溶剂
・有机物中的憎水基团:-R(烃基);烃基部分越大越难溶于水,亲水基团:-0H,-CHO,-
C0OH
・能溶于水的:低碳的醇、醛、酸、钠盐,如乙(醇、醛、酸)乙二醇、丙三醇、苯酚钠
・难溶于水的:烃,卤代烃,酯类,硝基化合物
・微溶于水:苯酚、苯甲酸
・苯酚溶解的特殊性:常温微溶,65℃以上任意溶
沸点
・同系物比较:沸点随着分子量的增加(即C原子个数的增大)而升高
・同类物质的同分异构体:沸点随支链增多而降低
・衍生物的沸点高于相应的烃,如氯乙烷〉乙烷・饱和程度大的有机物沸点高于饱和程度小的有机物,如脂肪〉油
・分子间形成氢键的有机物沸点高于不形成氢键的有机物如:乙醇〉乙烷
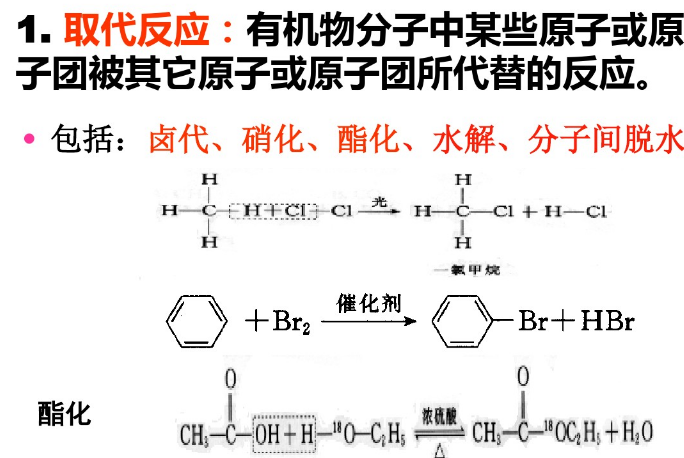
(三)有机化学反应类型
・有机反应主要包括八大基本类型:取代反应、加成反应、消去反应、氧化反应、还原反应、加聚反应、缩聚反应、显色反应,
有机反应类型――加成反应
・和H。加成的条件一般是催化剂(Ni)+加热
・和水加成时,条件写温度、压强和催化剂
・不对称烯烃或炔烃和H。0、HX加成时可能产生两种产物
・醛基的C=O只能和H。加成,不能和X,加成,而羧基和酯的C=O不能发生加成反应