大学化学mooc(天津大学)
第1章物质结构基础
1.1原子结构及核外电子的排布
1、微观粒子的特性粒二象性运动的统计性

第2章化学反应的能量关系
2.1基本概念
系统与环境
状态―→标准状态
状态函数及性质――强度性质和容量性质状态变化―过程只确定于始态与终态,与途径无关
2.2热力学第一定理
1、内能U热力学能
系统内部的原子和分子的各种形式能量的总和。
包括:分子振动、转动能;分子内原子的作用能―键能;电子的能量;质子运动的平动能;核内粒子间的作用能――核能.
3、焙H大多数过程都伴有P,V变化,故定义:
H=U+PV同样焙是状态函数,无法获得绝对值,只需求焙变AH.
4、焙变AH的计算
焙变AH在数值上等与可逆过程的热效应AH=Q可标准生成热(焙),ArH9标准燃烧热(焙),△.He


第3章化学平衡和化学反应速率
3.1、化学平衡


3.2、化学反应速率
化学反应速率的表示――反应进度
影响化学反应速率的因素

第4章溶液
4.1单相离子平衡
1、稀溶液的通性(依数性)只取决于溶质的粒子数


3、溶度积规则――比较J与kOsp的大小
4、溶度积的应用
沉淀的生成、沉淀的溶解、沉淀的转化
4.3配位平衡
1.基本概念配合物的组成配合物的命名
2.配离子的离解平衡
第5章电化学基础
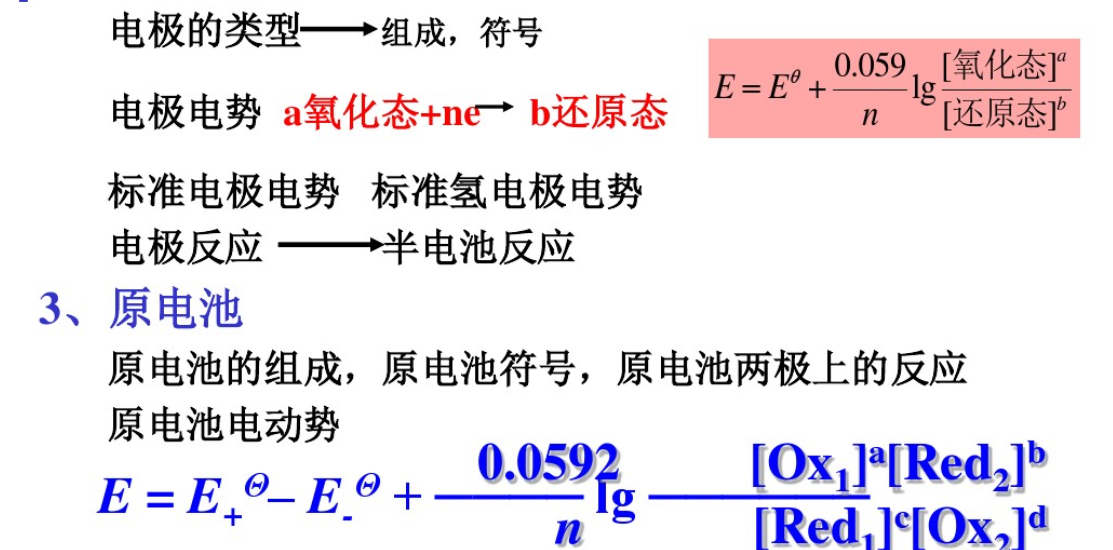
1、氧化数,氧化环原反应的配平,半反应,还原电对。
2、电极